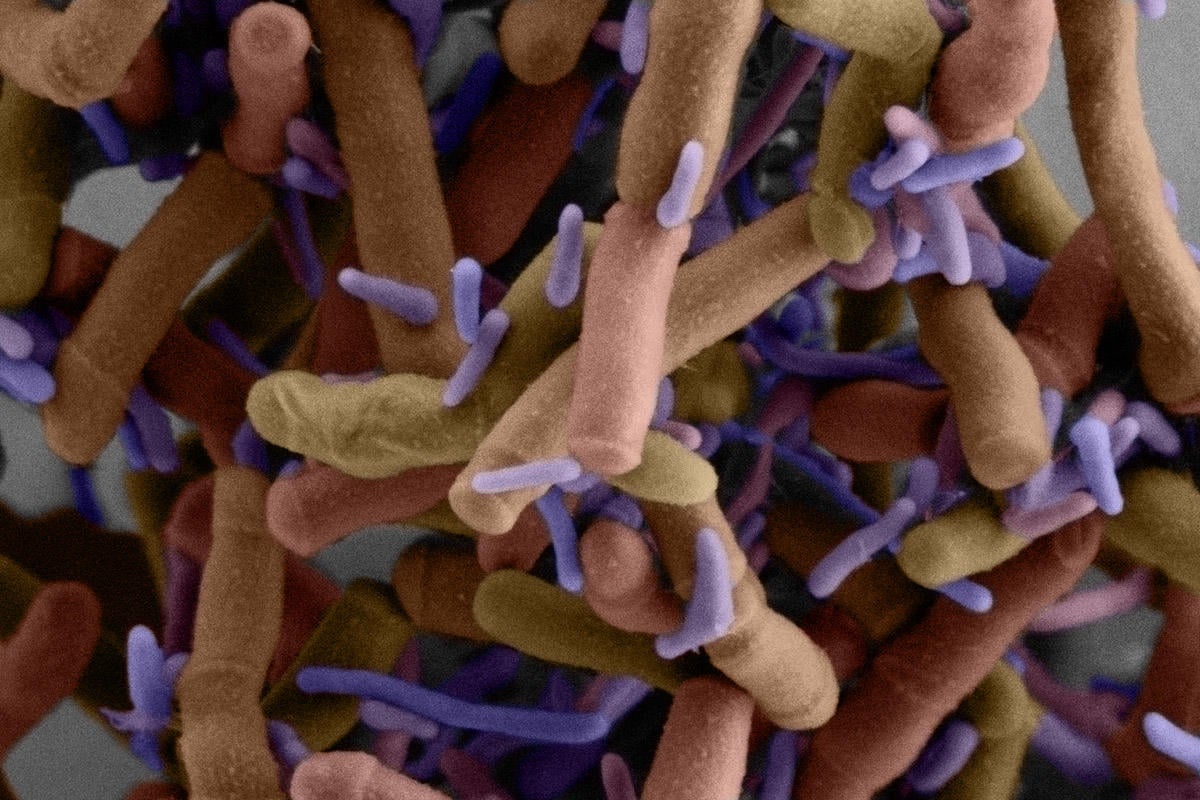

扫描电子显微照片显示,微小的紫色蝙蝠细菌细胞生长在大得多的细胞表面。 西雅图威斯康星大学医学院约瑟夫·莫戈斯实验室的新研究揭示了它们的生命周期、基因以及可能导致其不寻常生活方式的一些分子机制。 这种附生细菌是Southlakia epibionticum。 图片来源:Yaxi Wang、Wei-Pang Chan 和 Scott Braswell/华盛顿大学
科学家们发现了对生活在较大细菌表面的微小细菌的不寻常生活方式至关重要的基因。
蝙蝠细菌是一群神秘的微小微生物,其生存方式难以捉摸。 虽然科学家只能培育其中一些物种,但它们是在许多环境中发现的多样化家族的一部分。
研究人员可以在实验室中培养的少数巴氏杆菌驻留在较大宿主微生物的细胞表面上。 Patescibacteria 通常缺乏合成许多生命必需分子所需的基因,例如 氨基酸 构成蛋白质、构成细胞膜的脂肪酸以及它们所含的核苷酸 脱氧核糖核酸。 这使得研究人员推测其中许多细菌依赖其他细菌生长。
在最近发表的一项研究中 细胞研究人员首次了解了帕特西细菌异常生活方式背后的分子机制。 这一突破是由于发现了一种基因操纵这些细菌的方法而成为可能,这一进步开辟了一个潜在的新研究方向的世界。
尼廷·S. 说: “虽然宏基因组学可以告诉我们关于生活在我们身体上和体内的微生物的信息,但仅靠 DNA 测序并不能让我们深入了解它们的有益或有害活动,特别是对于以前从未被描述过的生物体,”该研究所的 Balija 说。 西雅图系统生物学博士,他为这项研究贡献了许多计算和系统分析。

表生细菌研究员 Larry A. 加拉格尔站在华盛顿大学医学院微生物实验室的显微镜前。 信用:S. 布鲁克彼得森/华盛顿大学
他补充说:“从基因上扰乱帕特西细菌的能力开启了应用强大的系统分析镜头来快速表征专性生物体的独特生物学特征的可能性。”专性生物体必须依靠另一种生物体才能生存。
进行这项研究的团队由大学微生物学系 Joseph Mougus 实验室领导 华盛顿大学 医学院和霍华德休斯医学院对 B. batischebacteria 感兴趣有几个原因。
它们是许多人们知之甚少的细菌之一,其 DNA 序列出现在对基因组的大规模遗传分析中。 分类– 来自环境来源的丰富微生物群落。 这种遗传物质被称为“微生物暗物质”,因为人们对其编码的功能知之甚少。
研究人员报告说,微生物暗物质可能包含有关具有潜在生物技术应用的生化途径的信息。 细胞 纸。 它们还包含支持微生物生态系统的分子活动的证据,以及该系统中不同微生物物种的细胞生物学的证据。
这篇最新论文中分析的 Patescibacteria 属于糖杆菌。 这些生物生活在各种陆地和水生环境中,但最出名的是栖息在人类的嘴里。 至少自中石器时代起,它们就一直是人类口腔微生物组的一部分,并与人类口腔健康有关。
在人类口腔中,酵母菌需要放线菌作为它们的宿主。 为了更好地了解酵母菌与宿主沟通的机制,研究人员利用基因操作来识别酵母菌生长所必需的所有基因。

西雅图华盛顿大学医学院微生物实验室厌氧工作站中的非生物细菌研究员王亚西。 信用:S. 布鲁克·彼得森/华盛顿大学
微生物学教授莫戈斯说:“我们非常高兴能够第一次了解这些细菌所具有的不寻常基因的功能。” “通过将我们未来的研究重点放在这些基因上,我们希望揭开酿酒酵母如何利用宿主细菌进行自身生长的谜团。”
研究中发现的潜在宿主相互作用因素包括可能帮助酵母菌附着在宿主细胞上的细胞表面结构以及可用于运输营养物质的专门分泌系统。
作者工作的另一个应用是产生表达荧光蛋白的糖杆菌细胞。 利用这些细胞,研究人员对与其宿主细菌共同进化的糖杆菌进行了延时荧光显微镜观察。
S.指出。 莫戈斯实验室的高级科学家布洛克·彼得森 (Brock Peterson) 表示:“酿酒酵母宿主细胞培养物的延时成像揭示了这种不寻常细菌的生命周期令人惊讶的复杂性。”
研究人员报告说,一些酵母菌通过附着在宿主细胞上并反复出芽来产生小群后代,从而充当母细胞。 这些小家伙继续寻找新的宿主细胞。 一些后代反过来变成了母细胞,而另一些似乎与宿主没有产生任何相互作用。
研究人员认为,进一步的基因操纵研究将为更广泛地了解他们所描述的“这些生物体所含有的丰富的微生物暗物质储备”的作用打开大门,并可能揭示尚未可视化的生物机制。
参考文献:“Patescibacteria 的基因操作为微生物暗物质和非生物生活方式提供了机制见解”,作者:Yaxi Wang、Larry A. Gallagher、Pia A. Andrade、Andi Liu、Ian R. Humphreys、Serdar Turkarslan、Kevin J. Cutler、Mario。 L. Arrieta-Ortiz、Yaqiao Li、Matthew C. Radey、Jeffrey S. McLean、Qian Cong、David Baker、Nitin S. Baliga、S. Brook Peterson 和 Joseph D. Mougous,2023 年 9 月 7 日,可在此处获取 细胞。
doi:10.1016/j.cell.2023.08.017
新成立的研究中心加强了这种跨学科和合作研究 微生物相互作用和微生物组中心 (缩写为 mim_c),由 Mojos 指导。 mim_c 的使命是通过与来自不同学科的志同道合的研究人员建立联系,减少微生物组研究的障碍并促进合作。 在这里,mim_c 成为 Mouugous 与威斯康星大学牙科学院牙周病学系口腔微生物组专家 Jeffrey McLean 一起加入实验室的催化剂。
这项研究的主要作者是威斯康星大学微生物学系的 Yaxi Wang 和 Larry A. Gallagher。 资深作者有 Baliga、Peterson 和 Mogus。 德克萨斯大学西南分校的生物化学家Qian Kong、威斯康星大学医学院的David Becker和其他研究人员也与麦克莱恩一起为蛋白质设计做出了贡献。
莫格斯和贝克是霍华德休斯医学研究所的研究人员。 Mogus 担任华盛顿大学 Lynn M. 和 Michael D. Garvey 主席。
该研究得到了以下机构的资助: 美国国立卫生研究院美国国家科学基金会、国防部国防威胁降低局、比尔及梅琳达·盖茨基金会和韦尔奇基金会。

“创作者。屡获殊荣的问题解决者。音乐布道者。无法治愈的内向。”





More Stories
詹姆斯·韦伯太空望远镜检测到超大质量黑洞附近的冲击(图片)
研究表明,富含水果和蔬菜的饮食可以降低患心脏病和肾脏疾病的风险
中国的巨大陨石坑里有“天堂”森林,其中的植物适应了严酷的地下生活